無細胞療法時代來臨-揭開幹細胞外泌體的神秘面紗
- Yield Healthy Life

- 4月17日
- 讀畢需時 7 分鐘

無細胞療法時代來臨! 揭開幹細胞外泌體的神秘面紗 間質幹細胞所分泌的外泌體逐漸引領一股無細胞療法的新趨勢。過往研究發現間質幹細胞所具備的多細胞分化潛力、抗發炎與免疫調節功能備受再生醫學領域重視,但使用細胞移植所面臨的腫瘤生成、微血管阻塞與免疫排斥等問題,使「無細胞」的治療手段逐漸成為研究焦點。源自間質幹細胞的外泌體屬於其中一種由細胞釋出的胞外囊泡,具有傳遞蛋白、mRNA、miRNA 及脂質等生物活性分子功能,亦有良好穩定性與免疫相容性,展現促進組織再生與調控免疫細胞的能力,研究顯示其實這也是間質幹細胞得以發揮其分化與調節免疫功能的主要參與介質。以下將詳細介紹間質幹細胞與其分泌之外泌體的類型、功能與應用價值,並簡短評估外泌體在再生醫療領域的市場可期性。
再生醫學上的新篇章——幹細胞療法
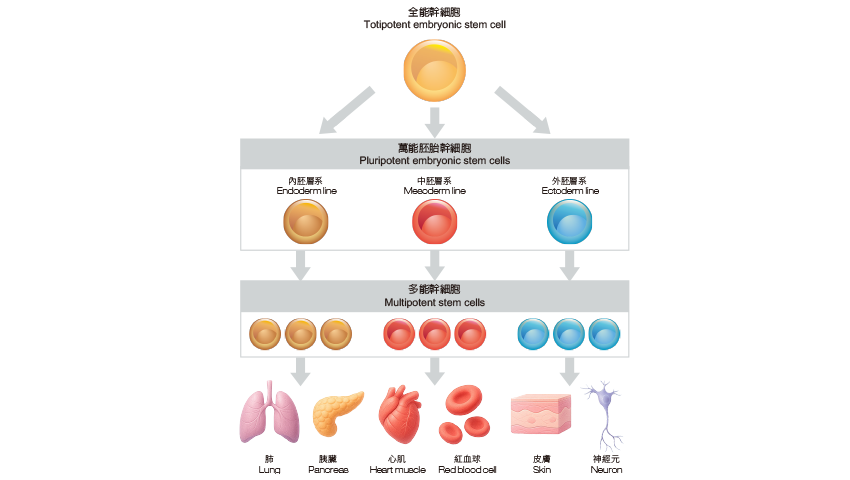
幹細胞是一群可不斷自我更新、增殖與分化的原始細胞,大部分存在於人體胚胎期,稱為胚胎幹細胞(embryonic stem cells, ESCs),此時期幹細胞的活動最為活躍,可接受各種分子訊號調控,藉從受精卵狀態逐漸分化至不同胚層,到一步步形成所有類型的體細胞,我們得以發育出完整而具生理功能的器官乃至個體。待胎兒出生後,體內雖仍保有部分幹細胞,其分佈範圍有所侷限,在分化能力上通常有細胞譜系(lineage)的限制,也就是僅能朝特定的細胞類型繼續分化發育,是謂成體幹細胞(somatic stem cells, SSCs),主要用於補充人體待死細胞,以維持器官組織的正常運作。一般而言,成體幹細胞亦會隨著年齡逐漸減少,因此孩童身體的組織修復能力總是較成年人佳。
成體幹細胞可進一步細分為造血幹細胞(Hematopoietic stem cells, HSCs)與間質幹細胞(mesenchymal stem cells, MSCs),前者分佈於骨髓與臍帶血,可生成所有類型的血球細胞;相對於造血幹細胞,間質幹細胞可分化為其他非血球類型的細胞,分布範圍也更加廣泛,如:胎盤、臍帶、骨髓、脂肪、牙髓等組織內。雖然間質幹細胞主要源自於囊胚的中胚層,但研究顯示,即使利用中胚層的骨髓或脂肪幹細胞,也可能透過適合的分子訊號調節,分化出屬於不同發育胚層的神經或肌肉細胞等,使得間質幹細胞的再生應用性大大提升,成為再生醫療領域的潛力股,不再受限於使用胚胎幹細胞所會面臨的倫理限制;遂間質幹細胞在分化類型、不同幹細胞所分化出的體細胞功能差異、操作步驟、以及各種疾病治療的可能性成為這十年來的研究重點,也有許多進入臨床試驗階段,更帶動相關產業發展,如:細胞工程、細胞儲存與運送、細胞療法。
間質幹細胞的旁泌作用
間質幹細胞具有強烈的趨化作用(homing),能在血液循環中辨識病灶部位,抵達後會在此處進行免疫調節(immune modulation)、召集並參與分化前驅細胞(progenitor cells)、與抵抗細胞凋亡(anti-apoptosis),且尤以降低免疫細胞活性的強大效果使其在許多創傷和慢性退化性疾病上具有治療優勢,能抑制炎症風暴,防止組織損傷擴大影響預後,並能啟動殘存細胞胞內的存活路徑,降低細胞死亡數量;在細胞修復的參與上,其實並不是直接由其分化成體細胞,更經常是透過一連串的訊號蛋白喚醒周圍的前驅細胞並徵召至病灶區,再將它們進一步增殖、分化為所需填補的細胞種類。
間質幹細胞主要是以旁泌作用(paracrine)的方式——藉由釋出不同的蛋白分子至鄰近細胞以啟動其胞內訊號來完成作用,其中包含大量的生長因子、趨化蛋白、以及包覆著多種訊息片段的胞外囊泡(extracellular vesicles, EVs);已有許多研究指出,若將間質幹細胞先經過移除滋養分泌物的前處理再進行體內移植,其再生修復效果就不復存,反之,若僅將其分泌物植入組織受損部位,將能獲得和幹細胞正常移植程序類似的療效,且此修復特性僅存在於間質幹細胞旁泌物,如使用的是成熟體細胞所分泌的蛋白分子則不具備修復作用。因此,解密間質幹細胞旁泌物與疾病治療機轉的關聯性是目前再生醫療領域的重點,這些研究結論攸關生物製劑的新藥開發,目的為取代傳統單一化學藥物無法解決的多靶效益和副作用問題。
間質幹細胞外泌體
間質幹細胞在參與組織修復上需仰賴複雜的訊號調控機制以及相關材料,其分泌的胞外囊泡會因幹細胞種類、應付的損傷組織不同,而製造並攜帶內容不盡相同的分子片段。與幹細胞的體積相比,這些囊泡僅有其百分之一甚至千分之一的大小,在血液循環中可較為自由穿梭而不會沈積在肺泡中,治療效率上較直接植入間質幹細胞佳。一般而言,這些胞外囊泡依形成機制與大小不同,可區分為下列兩種:
1.外泌體(exosomes)
直徑 30-150 nm,為最小的胞外囊泡,可攜帶大量生長因子與細胞激素如 EGFR、VEGF、TGFβ,及相關訊號的mRNA、miRNA,目前被視為能通過血腦障壁的小分子蛋白的運送載體。主要透過胞吐作用從多泡小體(Multivesicular bodies, MVB)釋出胞外,再由胞吞作用進入其他細胞。
2.微泡(microvesicles)
直徑比外泌體大,約 100-1000 nm。主要透過出芽作用釋出胞外,再經與其他細胞膜的融合作用將微泡中的訊息物釋放至胞內。
其中,外泌體是間質幹細胞所分泌的囊泡中研究最為廣泛的一類,其生物特性與治療潛力受到高度關注,間質幹細胞外泌體與其他細胞的外泌體類似,皆帶有結構上所需的蛋白質,以幫助外泌體接合、傳送訊息給目標細胞,這些蛋白因此可視為間質幹細胞外泌體的標記(biomarkers),不同來源的外泌體則包裹著該細胞的特殊蛋白與 RNA、DNA,甚至也帶有病毒 RNA。一般而言外泌體含有下列物質:
• 蛋白質
可作為幹細胞辨識指標的膜外蛋白如 CD9、CD63、CD81;多泡小體標記的HSP70、tetraspanins、Annexins、Alix、TSG101、黏附分子(ICAM-1)、酵素等,具有結構維持與訊息傳遞功能。
• 核酸
mRNA:在外泌體進入細胞後,可於受體細胞內轉譯成蛋白,進一步調控功能。
microRNA(miRNA):如 miR-21、miR-146a、miR-140-5p 等,可干擾目標細胞的mRNA,進而調節免疫反應、促進組織修復。
• 脂質
富含膽固醇、磷脂醯絲胺酸與神經醯胺,有助外泌體穩定存在並促進與細胞膜的融合。
雖然許多研究指出外泌體 RNA 與 miRNA 參與訊息傳遞的重要性,但事實上外泌體 RNA 多為短碎片、而 miRNA 甚至只佔 RNA 總量的 0.9%,因此間質幹細胞外泌體的細胞聯絡(cross-talk)仍以蛋白質為主、訊息片段做為受體細胞後續的機轉調控。而目前已解譯了上千種蛋白質可為外泌體攜帶。
間質幹細胞的「無細胞療法」(cell-free therapy)
目前已知使用間質幹細胞外泌體在治療應用上,具有低免疫原性(low immunogenicity)、可穿透組織屏障、趨化性強和穩定性較高等優勢。免疫原方面,因外泌體體膜表結構與宿主細胞相近,能避免被辨識為外來抗原,減少免疫排斥,比起幹細胞更適合用於異體治療;血腦障壁一直是中樞神經疾病治療上的一大障礙,不僅許多大分子藥物及細胞無法穿越,或因體循環關係而使分子結構降解而減低療效甚至失活,但受到外泌體包裹的各種小分子可以受趨化作用穩定無虞的穿越緊密組織,使生物製劑藥效能有效發揮,且其透過表面蛋白(如 integrins)能選擇性移動特定組織或病灶處,提升治療效率。綜合以上,分析不同來源細胞中外泌體所夾帶的蛋白質種類,可幫助我們有效率利用外泌體作為無細胞治療的取代工具。
而相較傳統細胞治療,使用外泌體亦具備許多醫療與製藥市場上的優勢:
1.生物安全性較高
因不含有細胞核或基因組,腫瘤生成、突變與異體排斥風險較低。
2.製程可望標準化
外泌體可經超高速離心、過濾、沉澱與層析純化等方法規格化且大量生產,適用 GMP 等級規範。無需如培養活細胞般相當倚賴細胞種類及分化步驟而有許多客製化的步驟。
3.保存與運輸方便
外泌體尺寸小、可做冷凍乾燥處理,無需在運輸過程監控溫度,對物流運送上較為便利。
4.法規接受度提高
間質幹細胞外泌體屬於「生物衍生物」,在大部分法規管理下可比照疫苗或血液製品辦理。
目前已有多家生技公司專注於外泌體平台技術開發,並陸續有產品進入新藥臨床試驗階段,顯示市場接受度逐年提高。根據市場研究報告指出,2025 年全球外泌體市場規模估值為約 2.22 億美元,至 2032 年預計將達 12.84 億美元,年複合增長率(CAGR)約為 28.5%;單就治療和診斷領域來看,2023 年此部分規模亦達約 5.5 億美元,預估至 2031 年將成長至約 19.9 億美元。全球相關市場正處於爆發式成長階段,間質幹細胞外泌體體作為再生醫學重點平台,在產業鏈中產品研發、治療應用、以及藥物載體等方面皆具主導地位。隨著可期之分離純化技術、載體平台與臨床研究數據增加,市場規模將會持續擴大,未來價值預計將超過數十億美元,屆時將有望成為再生醫學與個人化醫療的關鍵技術平台,並可能引領一波「無細胞療法」之醫學革命。

陳人輔 博士
現任世勛國際生醫股份有限公司創辦人暨科研總監|英國諾丁漢大學生物醫學博士|國立陽明大學口腔生物所碩士|致力於成人及胚胎幹細胞、再生醫學、幹細胞生長因子、美容再生醫學等相關領域進行研究與實際應用,曾於香港擔任亞太幹細胞研發副總及科技新報科學顧問




















留言